京都府立大学 大学院生命環境科学研究科 環境科学専攻
環境科学部 森林科学科
研究内容
木材構成成分およびその関連物質の化学反応性の微視的理解
木材は主に、セルロース、ヘミセルロースおよびリグニンという高分子成分から構成されています。セルロースとヘミセルロースは、D-グルコース、D-マンノース、D-キシロースなどの単糖がグリコシド結合で連結された成分で、これらは木材多糖と呼ばれます。リグニンは多彩な化学結合を含む芳香族高分子です。
木材の地上における存在量を考えると、これらの化合物は地上で最も豊富に存在する有機化合物と言えます。また、木材多糖やリグニンから誘導される様々な化学物質を含めると、木材構成成分に由来する化学成分の種類はさらに膨大なものになります。木材多糖とリグニン、またそれらの関連物質において進行する種々の化学反応を微視的・定量的に理解することは、基礎科学・応用科学の発展に大きく貢献するでしょう。
以下に、私たちの研究の一部をご紹介します。
リグニン側鎖の自動酸化における微視的機構の理解
リグニンの自動酸化(空気中の分子状酸素による酸化反応)は、古くより研究されている化学反応です。リグニンが地上で二番目に多い化学物質であること、分子状酸素が地球の大気の20 %を占めることを考えると、リグニンの自動酸化が人間活動を含む地球上の自然現象を説明する上で重要であることは明白です。またこのような純粋科学的観点だけではなく、リグニンの自動酸化を化学工業に応用することでリグニンと無毒なO2から社会において重要な様々な低分子化合物を作り出すことが可能です。図1に針葉樹リグニン中に含まれるβ-O-4型中間ユニットの、強アルカリ条件における自動酸化機構として提案されている反応経路を示します。この反応では反応物であるリグニンの芳香核側鎖が酸化分解されることで、低分子フェノール類であるバニリンが主要生成物として生成します。バニリンは、そのバニラ香料としての利用が有名ですが、医薬品原料などとしても利用される現代化学工業における基幹物質の一つです。私たちは、この自動酸化反応の精密制御法の開発を目的に、本反応におけるさらに詳細なメカニズムの解明を行っています。
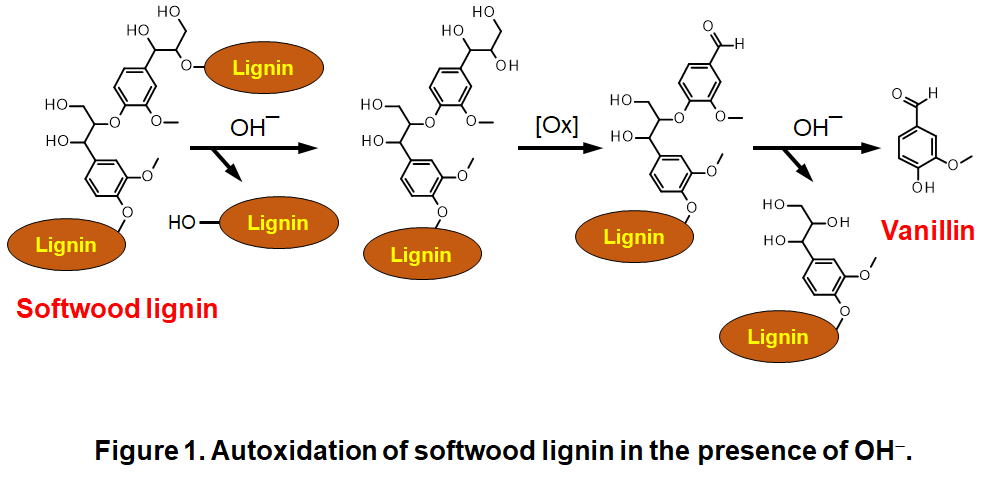
● Hirano, Y.; Izawa, A.; Hosoya, T.; Miyafuji, H. Degradation mechanism of a lignin model compound during alkaline aerobic oxidation: formation of the vanillin precursor from the β-O-4 middle unit of softwood lignin. React. Chem. Eng. 2022, 7, 1603-1616.
● Hosoya, T.; Yamamoto, K.; Miyafuji, H.; Yamada, T. Selective production of bio-based aromatics by aerobic oxidation of native soft wood lignin in tetrabutylammonium hydroxide. RSC Adv. 2020, 10, 19199-19210.
リグニンのアルカリ性ニトロベンゼン酸化における分子機構
アルカリ性ニトロベンゼン酸化(AN酸化)法は、木粉や様々な単離リグニン試料などのリグニン含有試料をニトロベンゼンにより強アルカリ下で酸化分解する方法です。AN酸化では、図2に示すようにリグニン試料中の芳香核の置換パターンを反映した4-ヒドロキシベンズアルデヒド類が主に生成します。これらの化合物の収率は、変性の少ないリグニン試料を用いた場合元々のリグニンの重量ベースで30~40%にも達します。リグニンの複雑な化学構造を考えるとこれは驚くべき高収率であり、このことからAN酸化法はリグニン分析法として古くから利用されています。AN酸化法は、現在のところ最も高選択的なリグニン分解法の一つですが、不思議なことにその分子機構はほとんど明らかにされていません。もしリグニン分析法として汎用されるAN酸化の分子機構が解明されれば、現在なお進行中であるリグニンの化学構造の全容解明に大きく貢献することが期待されます。また、リグニンを高選択的に分解するAN酸化のメカニズムが解明されれば、それを応用した新たなリグニンからの低分子化合物生産法の提案につながる可能性もあります。このような考えから、私たちはAN酸化におけるリグニン中の化学結合の切断機構やベンズアルデヒド類の生成機構の解明を、モデル化合物の分解実験や理論計算を駆使することで行っています。
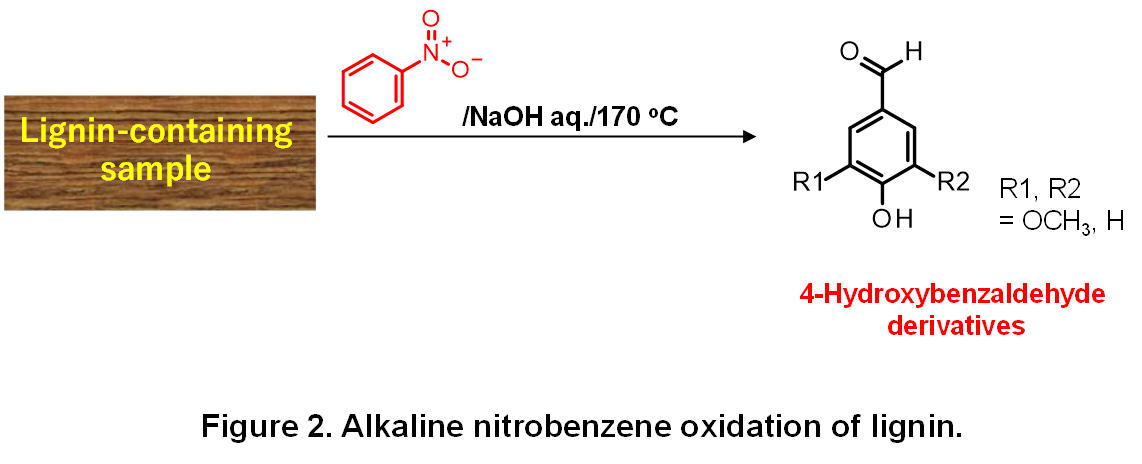
● Hayashi, T.; Hosoya, T.; Miyafuji, H. Vanillin production pathways in alkaline nitrobenzene oxidation of guaiacylglycerol-β-guaiacyl ether. J. Agric. Food Chem. 2023, 71, 10124-10132.
単糖類特にD-キシロースの合成化学的グリコシル化における定量的反応機構
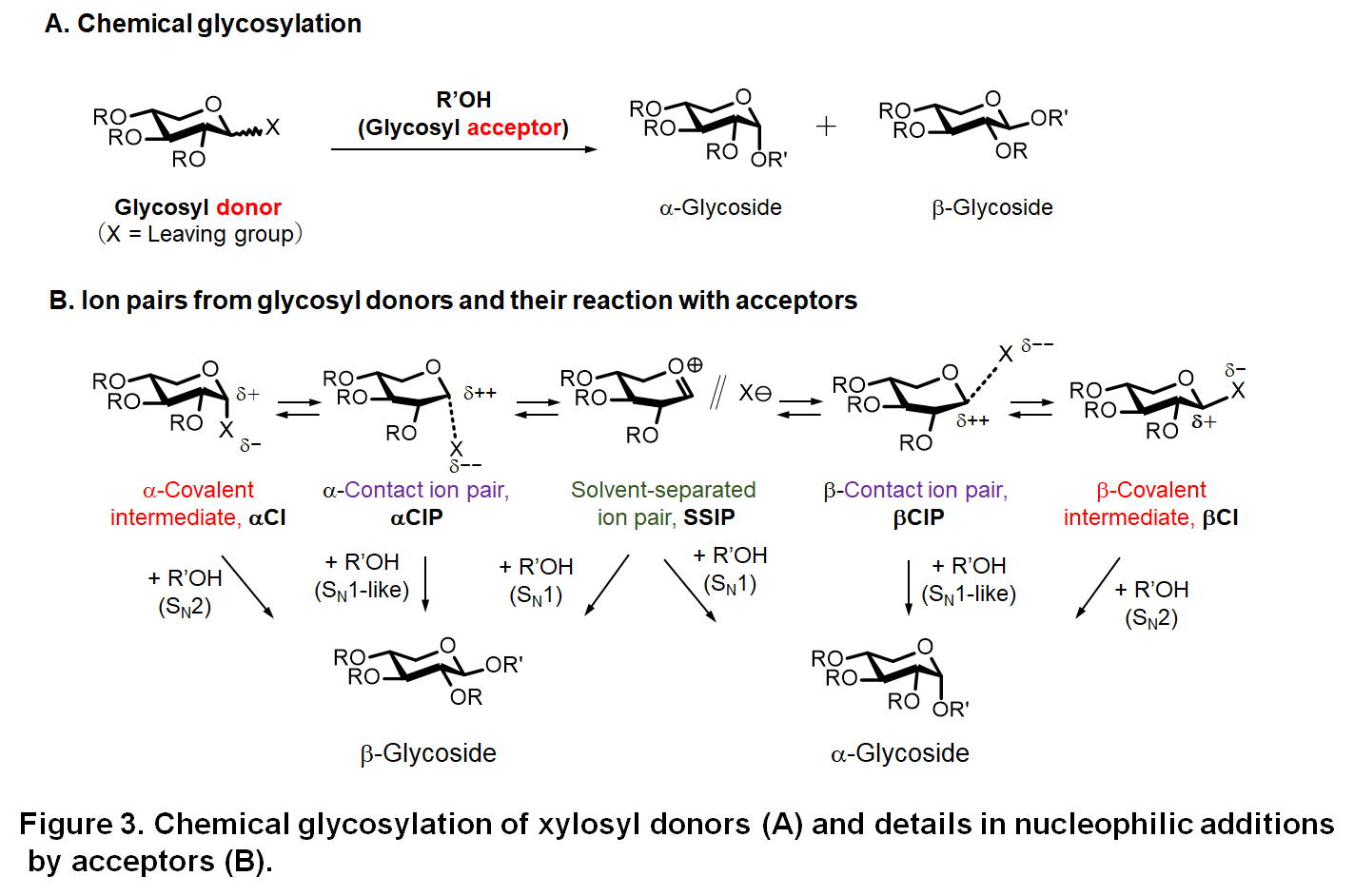
有機合成化学的グリコシル化反応(以下では単に「グリコシル化」とします)は、図3Aに示すように1位に脱離基Xを有する糖分子(グリコシルドナー)とアルコールなどの求核剤(グリコシルアクセプター)を反応させ、グリコシド類を合成するための反応です。この反応は、糖化学の分野で最も重要な反応のひとつで、様々な機能性糖分子の分子設計を行う上で不可欠なものです。木材化学においても、木材中の70 %がグリコシド結合によって単糖分子が連結された多糖成分であることからわかるように、グリコシル化反応は非常に重要な位置づけにあります。D-キシロースは木材(特にカンバ材などの広葉樹材)から比較的容易に取り出すことのできる単糖で、キシリトールなどの食品添加物の原料や化成品であるフルフラールの原料として利用されています。しかしながらこれらの用途は限定されたものであり、木材からの生産が容易なキシロースから医薬品などの高付加価値な分子を作り出せれば木材利用をさらに促進できると考えられます。そこで私たちはキシロースからの機能性糖分子の創出の基礎となる、キシロースのグリコシル化(キシロシル化)反応の詳細な分子機構の解明研究を行っています。
キシロシル化を含むあらゆるグリコシル化反応で問題となるのは、生成物の選択性です。図3に示すように、グリコシル化反応では一般にα/β体の両方のグリコシドが生成物として得られますが、合成上目的とされる生成物は通常どちらか片方のみです。したがって、不要な異性体の生成は目的物収率を低下させるのみならず、その後の目的物の分離精製を煩雑にしてしまいます。なぜグリコシル化反応の立体制御は困難なのでしょうか?― それはこの反応における反応機構の複雑性が一因です。図3Bに示すように、グリコシル化反応におけるフラスコの中では、ドナーと脱離基Xが共有結合した共有結合性中間体CIのみならず、そこから派生する緊密イオン対CIP、溶媒分離イオン対SSIPなどから構成される複雑な平衡混合物が生成し、各成分とアクセプター分子の間にSN2やSN1型の反応が進行するとされています。上記の立体選択性の制御には、この平衡を構成する各成分のアクセプターに対する反応性を理解し、その制御法について考える必要があるのですが、特にエネルギー的に非常に不安定なイオンペア類の化学的特性を明らかにするのは困難です。
このようなことを踏まえ、私たちの研究室では、グリコシル化反応の反応機構について、合成実験と理論計算を組み合わせた体系的研究を行っています。理論計算では、実験的な検討なほぼ不可能な不安定中間体や遷移状態の化学構造やエネルギーを評価することができます。私たちの研究によって、図3Bにおけるイオンペア類(X=OTf)の生成機構や共有結合性中間体との相対エネルギーなどが、世界で初めて理論的計算の視点から明らかにされています。今後は理論計算の結果を実験サイドからフォローすることで、グリコシル化反応の全体像が明らかになるものと期待されます。
● Hosoya, T.; Kosma, P.; Rosenau, T. Effects of a 4,6-diacetal protecting group on the stability of ion pairs from D-glucopyranosyl and D-mannopyranosyl triflates. Carbohydr. Res. 2015, 411, 64-69.
● Hosoya, T.; Kosma, P.; Rosenau, T. Contact ion pairs and solvent-separated ion pairs from D-mannopyranosyl and D-glucopyranosyl triflates. Carbohydr. Res. 2015, 401, 127-131.
● Hosoya, T.; Takano, T.; Kosma, P.; Rosenau, T. Theoretical foundation for the presence of oxacarbenium ions in glycoside synthesis. J. Org. Chem. 2014, 79, 7889-7894.